Стенд при инфаркте миокарда что это такое
Коронарное стентирование (сосудов сердца)
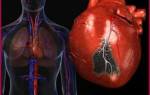
Основной причиной самого серьезного проявления ишемической болезни сердца, инфаркта миокарда, является нарушение питания мышцы за счет атеросклеротического поражения сосудов.
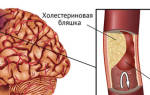
Атеросклероз поражает стенку артерии. Из-за потери эластичности теряется возможность к достаточному расширению. Отложение атеросклеротических бляшек изнутри вызывает сужение диаметра сосуда, затрудняет доставку питательных веществ. Критическим уменьшением считается 50% диаметра. При этом начинают проявляться клинические симптомы гипоксии (недостатка кислорода) сердца. Это выражается в приступах стенокардии.
Полная закупорка коронарной артерии ведет к развитию участка омертвения (некроза) при инфаркте миокарда. Во всем мире эта патология до сих пор считается одной из главных причин смертности взрослых людей.
Своевременное стентирование сосудов сердца позволяет предотвратить развитие тяжелых осложнений атеросклероза.
Что такое «стентирование»?
Термином «стентирование» называется операция по установке стента внутри артерии, в результате которой проводится механическое расширение суженной части и восстановление нормального кровотока к органу. Операция относится к эндоваскулярным (внутрисосудистым) хирургическим вмешательствам. Проводится в отделениях сосудистого профиля. Требует не только высокой квалификации хирургов, но и технической оснащенности.
В хирургии налажены методики не только коронарного стентирования (сосудов сердца), но и установка стентов в сонной артерии для устранения признаков ишемии мозга, в бедренной — для лечения атеросклеротических изменений ног, в брюшной аорте и подвздошной — при наличии выраженных признаков атеросклеротического поражения.
Что такое «стент», разновидности
Стент — это легкая сетчатая трубка, достаточно прочная, чтобы обеспечивать каркас артерии длительное время. Стенты изготавливаются из сплавов металла (чаще кобальта) в соответствии с высокими технологиями. Существует множество видов. Они отличаются по размерам, структуре сетки, характеру покрытия.
Можно выделить две группы стентов:
- без покрытия — используются при операциях на артериях среднего размера;
- покрытые специальной оболочкой из полимера, выделяющей в течение года лекарственное вещество, препятствующее повторному стенозу артерии. Стоимость таких стентов значительно дороже. Они рекомендованы для установки в коронарных сосудах, требуют постоянного приема лекарств, снижающих образование тромбов.
Как проходит операция?
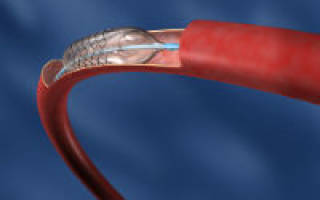
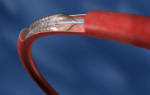
Для стентирования сосудов сердца в бедренную артерию вводится катетер, на конце которого располагается крошечный баллончик с надетым на него стентом. Под контролем рентгеновского аппарата катетер вводят в устье коронарных артерий и перемещают к необходимому участку сужения. Затем баллончик раздувается до необходимого диаметра. При этом атеросклеротические отложения вдавливаются в стенку. Стент, как пружина расширяется и оставляется на месте после сдувания баллона и удаления катетера. В результате — кровоток восстановлен.
Операция обычно проводится под местной анестезией. Длится от одного до трех часов. Перед операцией пациенту вводятся препараты, разжижающие кровь для профилактики тромбоза. При необходимости устанавливают несколько стентов.
После хирургического вмешательства больной проводит в стационаре до семи дней под наблюдением врача. Ему рекомендуется обильное питье для вывода с мочой контрастных веществ. Назначают антикоагулянты для предотвращения склеивания тромбоцитов и образования тромбов.
Кому показана операция, обследование
Отбором больных с ишемической болезнью сердца для оперативного лечения занимается консультант врач-кардиохирург. В поликлинике по месту жительства пациент проходит необходимый минимум обследования, включающий все обязательные анализы крови и мочи для определения функционирования внутренних органов, липограмму (общий холестерин и его фракции), свертываемость крови. Электрокардиография позволяет уточнить участки поражения миокарда после инфаркта, распространенность и локализацию процесса. Ультразвуковое исследование сердца наглядно на снимках показывает функционирование всех отделов предсердий и желудочков.
В стационарном отделении обязательно проводят ангиографию. Эта процедура заключается в внутрисосудистом введении контрастного вещества и серии рентгеновских снимков, проводимых по мере заполнения сосудистого русла. Выявляются наиболее пораженные ветки, их локализация и степень сужения.
Внутрисосудистое ультразвуковое исследование помогает оценить возможности стенки артерии изнутри.
Обследование позволяет ангиохирургу установить точное место предполагаемого внедрения стента, выявить возможные противопоказания к операции.
Показания для операции:
- тяжелые частые приступы стенокардии, определяемые кардиологом как предынфарктное состояние;
- поддержка аортокоронарного шунта (шунтирование — это установка искусственного кровотока в обход перекрытого сосуда), который имеет тенденцию к сужению в течение десяти лет;
- по жизненным показаниям при тяжелом трансмуральном инфаркте.
Противопоказания
Невозможность введения стента определяется во время обследования.
- Распространенное поражение всех коронарных артерий, из-за которого отсутствует конкретное место для стентирования.
- Диаметр суженной артерии меньше трех мм.
- Сниженная свертываемость крови.
- Нарушение функции почек, печени, дыхательная недостаточность.
- Аллергическая реакция пациента на йодистые препараты.
Преимущество стентирования перед другими операциями:
- малая травматичность методики — нет необходимости вскрывать грудную клетку;
- короткий период нахождения пациента в стационаре;
- сравнительно низкая стоимость;
- быстрое восстановление, возвращение к трудовой деятельности, отсутствие длительной инвалидизации больного.
Осложнения операции
Однако 1/10 часть прооперированных имели осложнения или нежелательные последствия:
- прободение стенки сосуда;
- кровотечение;
- образование скопления крови в виде гематомы на месте прокола бедренной артерии;
- тромбоз стента и необходимость повторного стентирования;
- нарушение функции почек.
Видео, наглядно показывающее суть операции:
Период восстановления
Перенесенное стентирование сосудов сердца позволяет намного улучшить самочувствие пациента, но это не останавливает атеросклеротический процесс, не изменяет нарушенный жировой обмен. Поэтому больному придется выполнять назначения врача, следить за уровнем холестерина и сахара крови.
Придется исключить из питания животные жиры и ограничить углеводы. Не рекомендуется употреблять в пищу жирную свинину, говядину, баранину, сливочное масло, сало, майонез и острые приправы, колбасные изделия, сыр, икру, макароны из нетвердых сортов пшеницы, шоколад, сладости и выпечку, белый хлеб, кофе, крепкий чай, алкоголь и пиво, газированные сладкие напитки.
Диета требует обязательно ввести в рацион овощи и фрукты в салатах или свежих соках, отварное мясо птицы, рыбу, каши, макаронные изделия из твердых сортов, творог, кисломолочные продукты, зеленый чай.
Необходимо наладить 5 – 6 разовое питание, следить за весом. При необходимости проводить разгрузочные дни.
Ежедневная утренняя гимнастика повышает обмен веществ, улучшает настроение. Нельзя сразу браться за тяжелые упражнения. Рекомендована ходьба, сначала на небольшие расстояния, затем с увеличением дистанции. Популярна медленная ходьба по лестнице. Можно заниматься на тренажерах. Обязательно пациентам следует научиться считать у себя пульс. Не допускать значительной перегрузки с учащением сердечных сокращений. Из видов спорта рекомендовано катание на велосипеде и посещение бассейна.
Лекарственная терапия сводится к средствам, понижающим артериальное давление (у гипертоников), статинам для нормализации уровня холестерина и препаратам, снижающим тромбообразование. Больным с сахарным диабетом следует продолжить специфическое лечение по назначению эндокринолога.
Лучше, если реабилитация после стентирования будет проводиться в санаторно-курортных условиях, под наблюдением медиков.
Операция стентирования проводится уже около сорока лет. Методика и техническое сопровождение постоянно усовершенствуются. Расширяются показания, нет возрастных ограничений. Рекомендуется всем пациентам с ишемической болезнью сердца не бояться консультации хирурга, это возможность продлить активную жизнь.
Реабилитация после инфаркта миокарда и стентирования
Современная медицина обладает различными методами лечения сердечных заболеваний, и один из них — стентирование, проводимое при инфаркте миокарда.Реабилитация после инфаркта миокарда и стентирования позволяет сохранить положительный результат и предотвратить появление осложнений после операции.
Показания и противопоказания
Стенд — это ультратонкая конструкция, напоминающая пружину. Ее устанавливают внутри сосуда в просвет коронарной артерии. При расширении она увеличивает просвет, обеспечивая нормальное кровообращение. Стентирование при инфаркте показано в следующих случаях:
- при заблокированных коронарных артериях (как при инфаркте, так и после него);
- при сужении одного или нескольких сосудов, что ведет к сбоям в работе сердца;
- при сужениях в сердечно-сосудистой системе, которые дают сбои в кровотоке, создают боли в груди, не исчезающие с принятием лекарств;
- при наличии острого коронарного синдрома.
Операция не имеет ряда противопоказаний, но перед ее проведением врач сопоставляет эффективность хирургического вмешательства и других методов лечения инфаркта миокарда. Если стентирование можно заменить лекарственной терапией или же другой операцией, то так чаще всего и делают. Установку стенда желательно заменить другим методом лечения в следующих случаях:
- если в скором будет проводиться операция, при которой возможны сильные кровотечения;
- если пациент в том возрасте, когда установление стенда нежелательно (до 22 или пожилой человек);
- если имеется запрет на антитромбоцитное лечение.
Виды стендов
Стентирование при инфаркте миокарда может проводиться с использованием различных видов стендов:
- BMS-стенды, изготавливаемые из металла. Они чаще остальных приводят к очередному сужению сосудов и осложнениям на сердце. У каждого третьего пациента, при операции которого использовались BSM-стенды, диагностируется повторное сужение артерий.
- DES пропитаны препаратами, которые начинают высвобождаться после установки стенда, предотвращая тем самым срастание соединительной ткани. Повторное сужение сердечных артерий при них возникает редко, но существует высокий риск возникновения тромбоза.
- Биоинженерные стенды покрыты антителами, оказывающими влияние на эндотелиальные клетки и притягивающими их к себе, уменьшая таким образом риск возникновения тромбоза.
- Биодеградируемые стенды при инфаркте постепенно растворяются в организме после установки, а содержащееся в них лекарство высвобождается и не дает сужаться сосудам.
- Стенды с двойным покрытием являются самыми дорогими, но в то же время наиболее эффективными. Они совместили в себе все достоинства DES и биоинженерных установок. Прогнозы при их установлении исключительно оптимистичные.
Как проводится процедура
Стентирование при инфаркте проводится в несколько этапов. Первым является подготовка к операции. Во избежание негативных последствий пациент должен:
- прекратить прием антикоагулянтов за 3 дня до стентирования, чтобы не возникло кровотечение;
- приостановить прием инсулина или лекарств для снижения уровня сахара в крови за несколько дней;
- не есть и не пить за 8 часов до хирургического вмешательства;
- выбрить паховую зону.
Также пациент проходит электрокардиограф и несколько других исследований.
Стентирование проводится с помощью ангиографа, который воспроизводит происходящее во время операции. Больной ложится на спину, его грудная клетка и конечности подключаются к электрокардиографу, а на предплечье устанавливается катетер для осуществления постоянного венозного доступа.
Вне зависимости от обширности инфаркта, пациент будет в сознании на протяжении всей процедуры. внутривенно ему будет введено сильное седативное средство, чтобы он был в спокойствии, немного сонливым, но способным общаться с хирургом. Проводится вмешательство в паховой зоне или в зоне предплечья, где находятся главные артерии.
Стентирование проходит следующим образом:
- зону, на которой будет проводиться операция, обеззараживают;
- в местную артерию вводится анестезия для того, чтобы проникновение иглой было неощутимо пациентом;
- в просвет иглы вводится проводник, после игла убирается;
- вводят катетер, который обеспечивает проникновение инструментов;
- через катетер вводится еще один, но меньшего размера, в нем и находится стенд в сложенном состоянии;
- стенд постепенно подводят к нужному месту;
- после того как стенд доходит до необходимого места, его раздувают баллоном для того, чтобы атеросклеротическая бляшка была прижата к стенкам артерии;
- катетер извлекается, а место введения сильно сжимается на 20 минут, после накладывается повязка.
Восстановительный период
После стентирования при инфаркте миокарда пациента помещают в реанимацию, где врачи наблюдают за его состоянием, артериальным давлением и работой сердца. Если при операции была задействована бедренная артерия, то больному необходим постельный режим. Ногу нужно держать в покое в течение 6 часов. Первый час после операции больной наблюдается каждую минуту. Если артерия была заклеена, то пациент будет лежать на несколько часов меньше, чем при стандартном сдавливании.
Если стентирование сосудов сердца проводилось на лучевой артерии, то необходимость постельного режима определяет лечащий врач. Сидячее положение можно занимать сразу после операции, если нет особых рекомендаций от хирурга. Начинать ходить можно лишь спустя 4 часа.
Пациенту, прошедшему стентирование после инфаркта, необходимо принимать много жидкости, так как в организм вводилось контрастное вещество. При учащенном мочеиспускании реагент будет выведен быстро.
После выписки из больницы необходимо продолжить восстановление в домашних условиях. Важным этапом в восстановлении является лечебная физкультура, начало проведения которой согласуется с врачом.
При средней тяжести заболевания ЛФК может начаться уже на 3 день от стентирования после инфаркта. При каждом повышении нагрузки на организм измеряется артериальное давление. При резком повышении показателей уровень нагрузки необходимо снизить.
Реабилитация после стентирования включает в себя коррекцию питания. Снижается калорийность пищи, пациент ограничивает себя в мучных, сладких, жирных, чрезмерно соленых и острых продуктах, обязательно увеличивается количество жидкости, а приемы пищи становятся более частыми, но порции при этом уменьшаются. Основой рациона должны стать следующие продукты:
- нежирное мясо;
- свежие овощи и фрукты;
- домашние соки и компоты без добавления сахара;
- хлеб ржаной или с отрубями;
- рыба;
- вареные яйца;
- молочные продукты.
В первые дни врачи рекомендуют употреблять только перетертую пищу, которая не требует пережевывания.
В период восстановления после инфаркта и стентирования пациенту можно выполнять не всю работу по дому, в зависимости от тяжести заболевания. Следует избегать неудобного положения тела и переутомления. Половую жизнь можно начинать после 1,5 месяцев после проведения операции. При этом необходимо держать рядом нитроглицерин. Перед актом нельзя принимать алкоголь, энергетические напитки и париться в горячей ванной.
Стенд при инфаркте миокарда что это такое
В лечении острого инфаркта миокарда (ОИМ) главной целью является восстановление кровотока в инфаркт-связанной коронарной артерии (КА), что подтверждается научными и клиническими данными.
Скоординированная региональная стратегия оказания помощи при инфаркте миокарда (ИМ) может значительно сократить время до начала лечения. Сортировка больных и включение в оказание помощи специалистов по проведению реперфузии должны начинаться при первом медицинском контакте с больным. Перенос момента записи ЭКГ и ее расшифровки из ОНП на догоспитальный этап (т.е. в машине НМП) может заметно уменьшить временной период «дверь-баллон».
Тактика, включающая и интервенционную, и фармакологическую реперфузию на догоспитальном этапе, может быть успешной в некоторых населенных пунктах. Однако простой алгоритм селективной реперфузии может осложнятся рядом обстоятельств, связанных с пациентом или с местными техническими ресурсами. В регистре NRMI-4 большая госпитальная специализация с первичным ЧКВ ассоциируется с более коротким временным периодом «дверь-баллон» и более низкой смертностью.
Похоже, что только первичное ЧКВ улучшит клинические исходы.
В медицинском учреждении проведение первичной интервенционной стратегии нуждается в мультидисциплинарном подходе. По прибытии в госпиталь оценку больного следует проводить быстро и в полном объеме, используя точные протоколы и эффективное взаимодействие персонала, чтобы обеспечить быстрое поступление пациента в отделение катетеризации.
При оценке коморбидных состояний нужно сосредоточиться на болезнях сосудов, аллергии, ФР антикоагуляции, функции почек, возможной беременности и функциональном статусе. Лечение ИМ следует начинать быстро (включая аспирин, гепарин и β-АБ или нитраты при показаниях). Нет ни одного рандомизированного исследования по оценке [3-АБ, вводимых в/в пациентам с первичным ЧКВ. Наблюдательные исследования показывают, что β-АБ при первичном ЧКВ могут уменьшать риск желудочковой тахикардии, фибрилляции желудочков во время процедуры и показатели смертности.
Необходима осторожность при в/в введении β-АБ пациентам с критическим гемодинамическим статусом из-за риска кардиогенного шока, что было показано в большом исследовании COMMIT (Clop >
После катетеризации нужно обеспечить оказание дальнейшей интенсивной медицинской помощи. Соответствующие протоколы предусматривают специализированную помощь, но возможны различные осложнения. В большинстве случаев первичное ЧКВ — более сложное вмешательство, чем плановое, поэтому лицо, проводящее процедуру, должно обладать достаточными профессиональными знаниями об ОИМ.
Гепарин остается стандартным антитромбиновым агентом, используемым при первичном ЧКВ, но продолжаются исследования по оценке бивалирудина. В недавно закончившемся исследовании OASIS-6 (Organization to Assess Strategies for Ischemic Syndromes) использование при первичном ЧКВ ингибитора фактора Ха фонда-паринукса привело к большей частоте тромбозов катетера.
Подготовка обоих бедренных доступов — простая превентивная процедура. При ангиографии внимание должно быть обращено на наличие коллатерального кровотока, чтобы была возможность провести вмешательство в инфаркт-связанной коронарной артерии (КА). Ангиографию артерии можно выполнить с помощью проводникового катетера, но следует соблюдать осторожность при проведении проводника в главном сосуде при наличии его окклюзии. Если расположение проводника не приводит к реперфузии и адекватной визуализации, следует использовать баллонный катетер соответствующего размера.
Медиана индекса сохраненного миокарда по терцилям временных интервалов лечения.
Было отмечено уменьшение индекса сохраненного миокарда в зависимости от времени в группе ТЛТ (р = 0,03), но не в группе стентирования (р = 0,59).
Нужно обратить внимание на возникновение преходящих реперфузионных аритмий и гипотонии. При адекватной визуализации можно использовать прямое стентирование, если нет бифуркационного поражения или выраженной кальцификации. Небольшое рандомизированное исследование (n = 206) показало, что прямое стентирование в сравнении с баллонной предилатацией приводит к более быстрому снижению сегмента ST. Бифуркационные повреждения — это проблема при проведении первичного ЧКВ. В недавнем исследовании 276 пациентов боковые ветви часто перекрывались стентом, который был установлен в основном сосуде (29%).
Острая окклюзия боковых ветвей возникала в 12,5% случаев. Бифуркационное стентирование при ОИМ является существенным ФР тромбоза стента.
Серьезными ограничениями реперфузионной терапии остаются дистальная эмболизация и ухудшение перфузии миокарда. Рутинное применение тромбэктомии или устройств дистальной защиты пока себя не оправдало. Селективному применению таких устройств могут помочь ряд признаков, выявляемых с помощью ангиографии или ВСУЗИ. Если дистальная эмболизация или феномен no reflow возникает во время вмешательства, для улучшения перфузии миокарда используют внутрикоронарное введение вазодилататоров. В недавнем сравнительно небольшом (n = 40) исследовании внутрикоронарное введение нитропруссида привело к лучшей реперфузии, выявляемой ангиографически, по сравнению с аденозином или верапамилом.
В некоторых ситуациях возникновение феномена no reflow может привести к серьезному ухудшению гемодинамики. Для улучшения кровотока у пациентов с рефрактерным феноменом no reflow использовали внутрикоронарное введение норадреналина, что может служить адекватным подходом к лечению пациентов с гипотензией. Эти вещества действуют преимущественно в дистальных отделах эпикардиальных сосудов.
Многососудистое поражение встречается у 40-65% пациентов с ОИМ. Множественные комплексные коронарные нарушения, такие как тромб, изъязвление, нерегулярный или нарушенный кровоток, были выявлены у 40% пациентов с ОИМ и могут быть отражением системного процесса с наличием большого количества уязвимых АБ. Наличие множественных сложных АБ связано с большим количеством повторных ишемических событий.
Обычный подход к пациенту с ИМ и многососудистым поражением включает экстренную хирургию, ангиопластику, отсроченную хирургию или неинвазивную оценку после реперфузии. Современные методы ангиопластики позволяют проводить многососудистую реваскуляризацию во время первичной процедуры. Однако в современных руководствах АСС/AHA рекомендуется избегать вмешательств на артерии, не связанной с ИМ и не влияющей на состояние гемодинамики. Рандомизированных исследований по оценке ЧКВ при ОИМ с многососудистым поражением проведено недостаточно.
В серии первичных ЧКВ у 820 пациентов при многососудистом поражении было больше крупных неблагоприятных СССоб в течение 1 года (31% vs 13%, р